- TECHNOLOGY
- DeepZema®
DeepZema®
DeepZema®는 최적의 신약후보물질 발굴을 위한 인공지능 플랫폼입니다.
신약 연구개발은 시간적, 비용적 소모가 큰 과정입니다. 신약 하나를 시장에 출시하기 위해서, 바이오∙제약 기업들은 일반적으로 10-15년 동안 10억 달러 이상을 지출합니다.
기존의 신약연구 방식에서는, 하나의 약물 후보를 찾는데 4-5년이 걸릴 수 있습니다. 향후, 신약 연구 개발 과정에서 시간과 비용을 줄이는 기술을 가진 기업들이 업계를 선도할 것입니다.
지난 몇 년간, 제약산업에서는 Insilico Medicine 社(미국) 및 Exscientia 社(영국) 같은 인공지능 기반의 신약 개발 스타트업(Start-up) 기업들이 엄청난 성장을 보여 주었습니다.
이 기업들이 사용하는 인공지능 기반 기술의 공통된 특징은 (1) 오믹스 기반의 질병 관련 타겟 발굴(omics-based identification)과 (2) 생성 모델을 사용한 다중 매개변수 선도물질 최적화(multi-parameter lead optimization)입니다. 인공지능 기술이 확실히 신약 발굴 과정을 도와주기는 하지만, 소규모 스타트업이 감당할 수 없는 큰 규모의 재정 및 인적 자원을 요구하는 경우가 많습니다.
㈜이노보테라퓨틱스는 이런 문제들을 해결하고자, 기존의 컴퓨터를 이용한 신약개발 기술에 인공지능 기술을 더하여 훨씬 실용적인 방식을 도입하였습니다. ㈜이노보테라퓨틱스의 기술은 머신러닝(Machine Learning)을 기반으로 하여 타겟발굴과 ADME/Toxicity 예측이 가능합니다. 신규화합물 생성을 위한 강화학습에 초점을 맞추는 대신, ㈜이노보테라퓨틱스는 기존의 de novo 디자인과 docking을 조합하여 새로운 구조를 생성합니다. 이후 딥러닝(Deep Learning) 기반의 평가함수를 이용하여 설계된 구조들의 결합형태를 평가하고 ADME/Toxicity 특성을 예측하여 최적화에 활용합니다. 이 모든 계산 과정을 결합하여 ㈜이노보테라퓨틱스만의 고유한 컴퓨터 플랫폼인 DeepZema®가 만들어졌습니다.
DeepZema®는 (1) 단순함 (2) 민주성 (3) 실용성으로 구성된 3가지 철학을 가지고 개발되었습니다. 이 철학을 바탕으로, DeepZema®는 전문가와 비전문가 모두가 쉽게 접근할 수 있는 간단한 웹 인터페이스를 가지고 있으며 실시간으로 결과를 알 수 있습니다. DeepZema®는 서버가 데이터베이스 및 컴퓨팅 엔진에 연결되어 있는 일반적인 서버-클라이언트 시스템으로 구성됩니다.
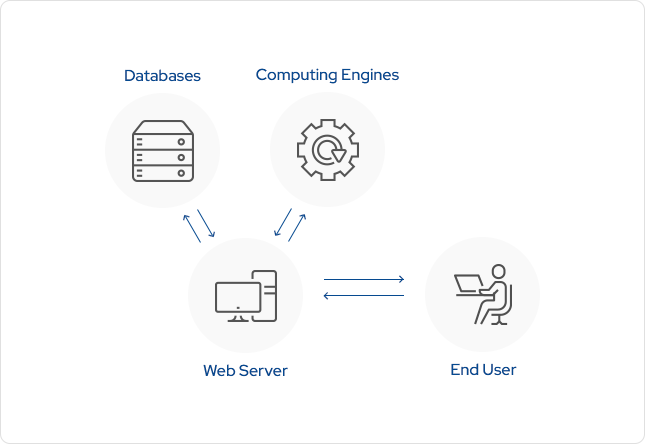
DeepZema®는 신약연구의 전 과정에 활용이 가능합니다.
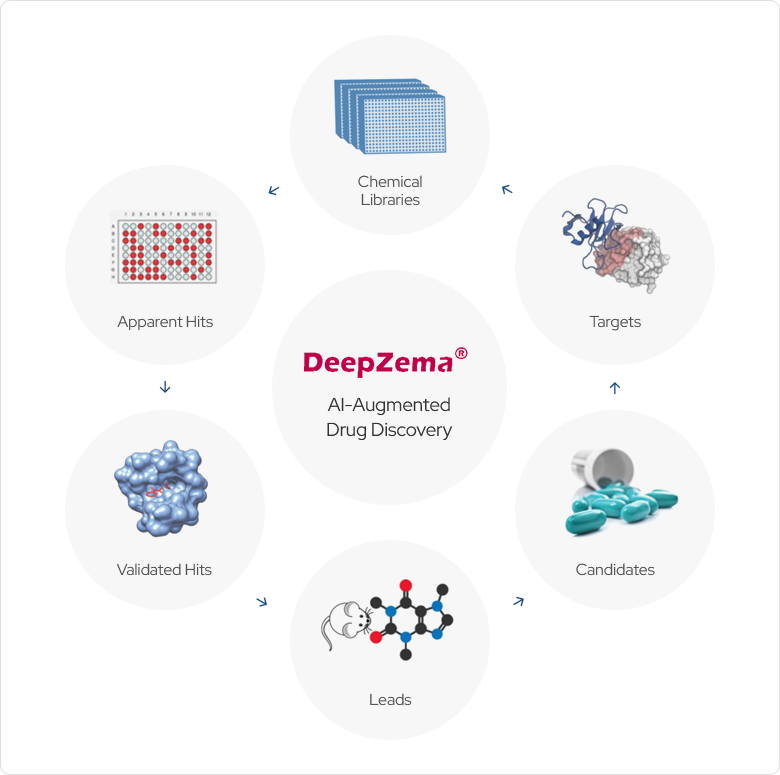
- • Ligand similarity and shape-based target identification.
- • Browsing/searching internal/external databases such as Dotmatics,
PubChem, ChEMBL, PDB, DrugBank and ChemBank. - • Virtual screening of chemical libraries and hit confirmation
(identification of false positives). - • Conformational analysis and 3D shape alignment of ligands.
- • Lead optimization (QSAR, de novo design, protein-ligand docking)
- • ML-based ADME/Toxicity calculations
- • Developability assessment (melting properties, pH dependence of solubility,
permeability, formulation, etc) - • Project management (current status report, etc)
DeepZema®가 어떻게 작동하는지 몇 가지 예를 소개하겠습니다.
- Kinome Profiling
- Target Prediction
- ADME/Toxicity Prediction

Kinase inhibitor를 개발할 때, 원하는 효능과 안전성 수준을 얻기 위해서는 전체 kinome에 대한 selectivity profiling이 매우 중요합니다. DeepZema®에 구현된 kinome profiling 모듈 덕분에, 합성 전에 화합물의 kinome selectivity profiling을 확인할 수 있습니다.
실례로, Syros pharma 社(미국)의 CDK7 inhibitor 최적화 과정에서, SY-5609과 SY-5102 모두 높은 CDK7 활성(activity)을 보여줬지만 485개의 kinase panel screen에서는 SY-5609가 훨씬 더 좋은 selectivity profiling을 보였기에 SY-5609가 개발 후보로 선정되었습니다 (J. Med. Chem. 2022, 1458).
DeepZema® kinome profiling을 사용하면, 이 상황을 위와 같이 쉽게 재현할 수 있습니다. 이는 DeepZema®의 kinome profiling 기능이 후보물질 발굴 과정에서 selectivity optimization을 도와줄 수 있음을 의미합니다.
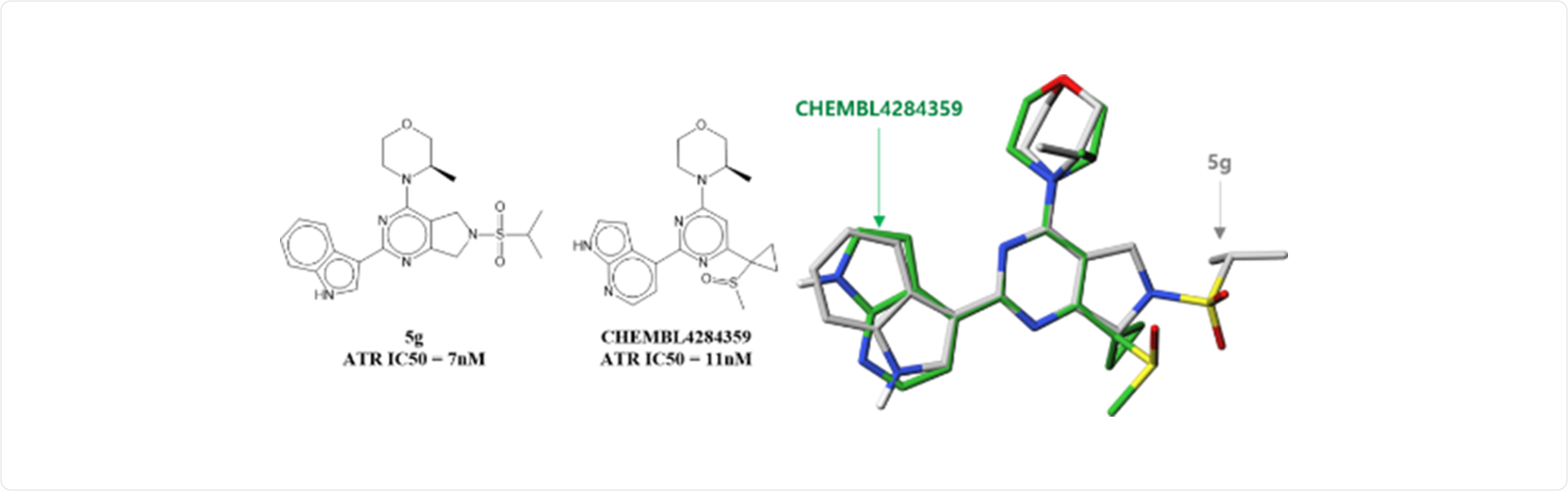
DeepZema®는 타겟 예측을 위한 두 가지 접근 방식을 제공합니다 (예, 등각 예측(conformal prediction)과 3D 구조 매칭(3D shape matching)). 위 그림의 화합물 ‘5g’은 IC50가 7nM인 ATK kinase inhibitor입니다 (BMCL 2022, 1t28651). 등각 예측을 이용하면 mTOR 및 ATR이 ‘5g’ 화합물에 대해 알맞은 타겟이라고 보여줍니다. 반면에, ‘5g’ 화합물의 3D shape alignment는 기존의 kinase inhibitor library에 대해 mTOR, PI3K, CLK4, MAPK1 및 ATR kinase와 같은 여러 kinase를 보여주었습니다. 타겟 예측은 표현형 스크리닝 히트의 타겟(Phenotypic screening hits)을 확인하거나 화합물의 off-target 확인을 위해 사용됩니다.
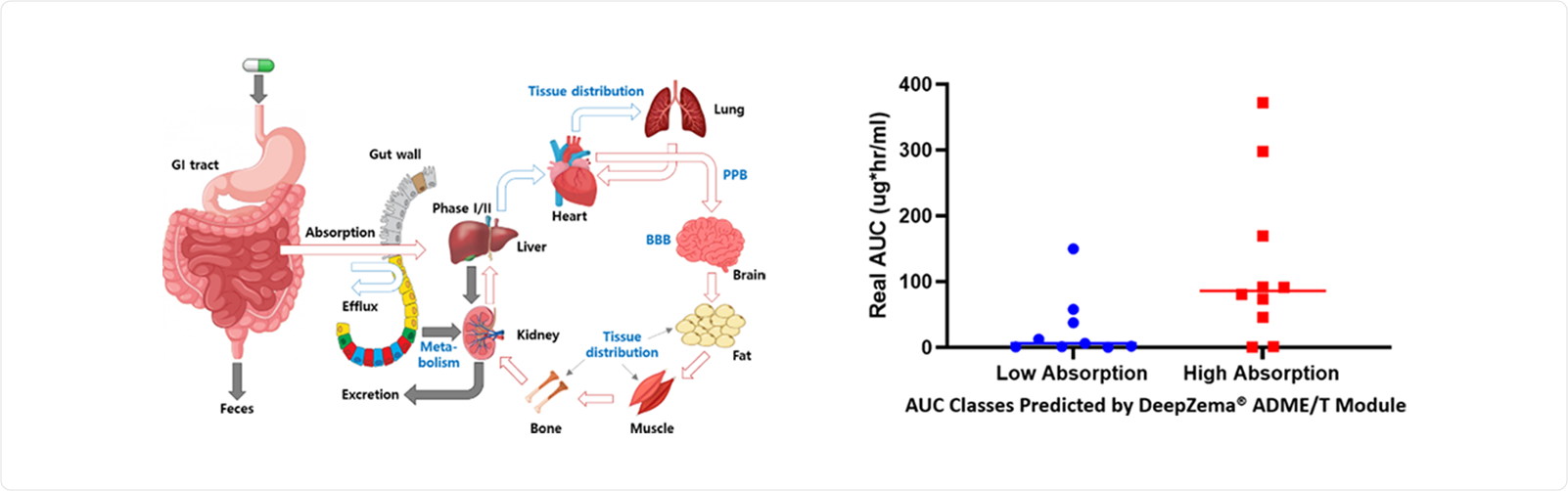
위 그림은 약물의 경구투여시 ADME(Absorption, Distribution, Metabolism and Excretion)를 보여줍니다 (Predicting ADME Properties of Chemicals, K. T. No et al, Springer 2017). 경구투여된 약물은 ADME 특성이 매우 중요하고 ADME 특성은 약물이 표적 기관에 도달하여 약리학적 효과를 나타내도록 최적화되어야 합니다. 신약연구 초기 단계에, in silico 방식은 선도물질 최적화 단계에서 ADME 평가 시간과 비용을 줄여줍니다.
위 그림에서 볼 수 있듯이, DeepZema®의 모듈은 흡수력이 높은 화합물과 낮은 화합물을 명확히 구별할 수 있을 만큼 신뢰할 만한 결과를 보여주고 있습니다.
